统计力学在生物体系的简单应用
回顾(接上次)
- 微观态:各组分微观排列的一个特定实现
- 溶液格子模型(a lattice model of solution)
- 计算:组合数
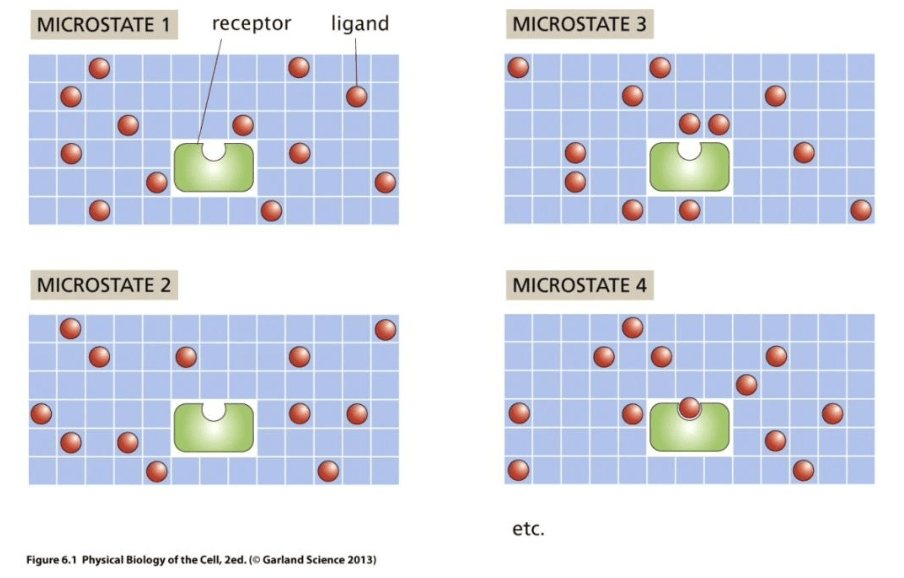
熵与疏水性质(hydrophobic)
- 氢键
- 静电力(90%)
- 共价键(10%)与电子云的交叠有关
疏水性质来源于:水的某些构型不被允许
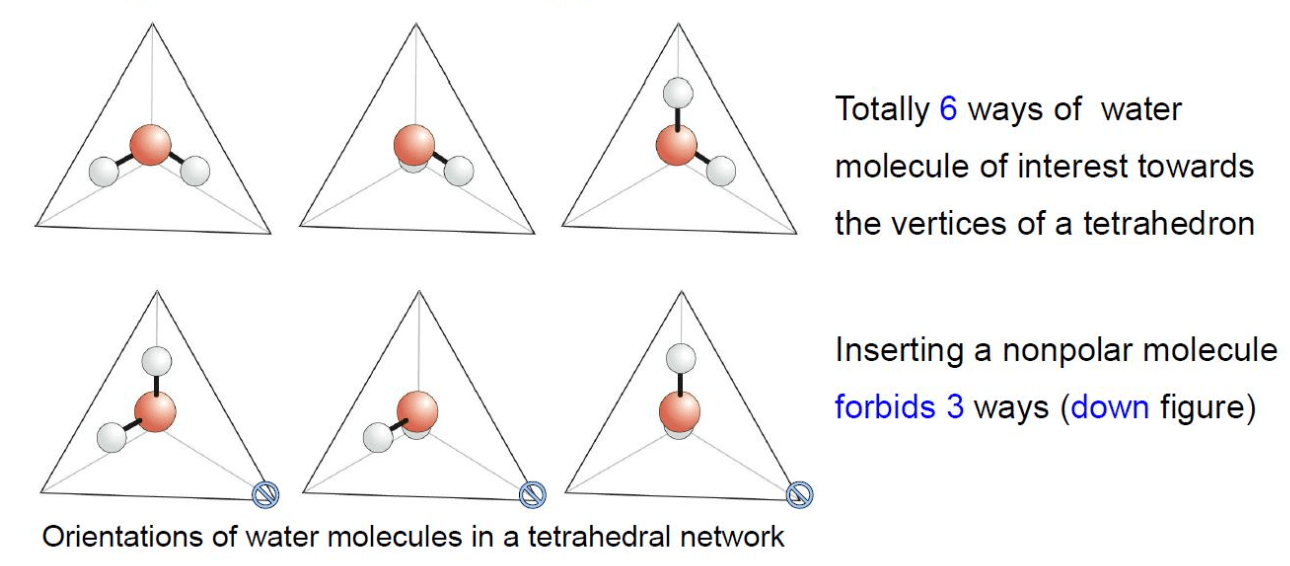
单个水分子的熵改变:
\[ \Delta S = \underset{\text{有约束 }\mathrm{H_2O}}{\underbrace{k_B \ln 3}} - \underset{\text{无约束 }\mathrm{H_2O}}{\underbrace{k_B \ln 6}} = - k_B \ln 2 \]
Estimate: interfacial energy of a hydrophobic object in water
\(\gamma\): free energy per unit area for a hydrophobic molecule
配分函数的物理意义
类似于分析力学里的哈密顿量,有了配分函数,就可以求出系统的各种热力学量,是统计力学的“分析机”(analytical engine)。
Ligand-receptor binding
水合自由能 \(\varepsilon_{\text{sol}}\):溶质分子与水的相互作用能量
忽略溶质分子与受体的相互作用能量,考虑溶液格子模型。未与受体位点结合的体系能量为 \(L \varepsilon_{\text{sol}}\). 结合后能量为 \((L - 1) \varepsilon_{\text{sol}} + \varepsilon_{\text{bind}}\).
\[ \frac{\Omega!}{(\Omega - L)!} \approx \frac{\Omega^L}{L!}, \quad \text{for } L \ll \Omega \]
Binding Curve
\[ p_{\text{bound}} = \frac{(L/\Omega) e^{-\beta \Delta \varepsilon}}{1 + (L/\Omega) e^{-\beta \Delta \varepsilon}} \xrightarrow[c_0 \equiv \Omega/V_{\text{tot}}]{c \equiv L/V_{\text{tot}}} \frac{c e^{-\beta \Delta \varepsilon}}{1 + c e^{-\beta \Delta \varepsilon}} \]
Osmotic pressure
细胞外液渗透压 90% 以上来自 \(\mathrm{Na}^+, \mathrm{Cl}^-\)
考虑一个有半透膜格挡的容器,膜两侧分别是纯水和溶解了大分子的溶液
平衡态:\(\mu_{\mathrm{H_2O}}^L = \mu_{\mathrm{H_2O}}^R, T_L = T_R = T\)
右侧隔室
\[ G_{\text{tot}}(T, p, N_{\mathrm{H_2O}}, N_s) = N_{\mathrm{H_2O}} \mu_{\mathrm{H_2O}}^0(T, p) + N_s \varepsilon_s (T, p) + k_B T \left( N_s \ln \frac{N_s}{N_{\mathrm{H_2O}}} - N_s \right) \]
故
\[ \mu_{\mathrm{H_2O}}(T, p) = \left( \frac{\partial G_{\text{tot}}}{\partial N_{\mathrm{H_2O}}} \right)_{T, p} = \mu_{\mathrm{H_2O}}^0(T, p) - \frac{N_s}{N_{\mathrm{H_2O}}} k_B T \]
左右隔间的水化学势:
\[ \left \{ \begin{aligned} & \mu_{\mathrm{H_2O}}^L = \mu_{\mathrm{H_2O}}^0(T, p_L) \\ & \mu_{\mathrm{H_2O}}^R = \mu_{\mathrm{H_2O}}^0(T, p_R) - \frac{N_s}{N_{\mathrm{H_2O}}} k_B T \approx \mu_{\mathrm{H_2O}}^0(T, p_L) + \frac{\partial \mu_{\mathrm{H_2O}}^0}{\partial p} (p_R - p_L) - \frac{N_s}{N_{\mathrm{H_2O}}} k_B T \end{aligned} \right. \]
由平衡条件 \(\mu_{\mathrm{H_2O}}^L = \mu_{\mathrm{H_2O}}^R\) 可得
稀溶液渗透压是一种熵力,与溶质种类、大小无关
Estimate: Osmotic pressure in an E. coli(大肠杆菌)cell
大肠杆菌内的典型无机盐浓度为 \(100 \, \mathrm{mM}\)
\[ \frac{N_s}{V} = \frac{100 \times 10^{-3} \times (6 \times 10^{23})}{10^{-3} \, \mathrm{m^3}} = 6 \times 10^{25} \, \mathrm{m^{-3}} = 6 \times 10^7 \, \underset{\text{细胞体积约 1 fL}}{\mathrm{ions}/\textit{E. coli}} \]
则内外渗透压差
\[ \Delta p_{\text{ion}} = p_{\text{in}} - p_{\text{out}} = \frac{N_s}{V} k_B T = (6 \times 10^{25}) \times (4.1 \times 10^{-21}) \, \mathrm{Pa} = 2.46 \times 10^5 \, \mathrm{Pa} = 2.46 \, \mathrm{atm} \]
热力学角度看理想气体的压强:熵力
对于准静态等温过程,气体的内能不变,膨胀过程可视作熵增的后果
\[ \mathrm{d} U = T \mathrm{d} S - p \mathrm{d} V = 0 \implies p = T \left. \frac{\partial S}{\partial V} \right|_{T, N, \ldots} \]
压强与 \(\frac{\partial S}{\partial V}\) 成正比,熵有自发增加的趋势,也就自然产生了压强。

